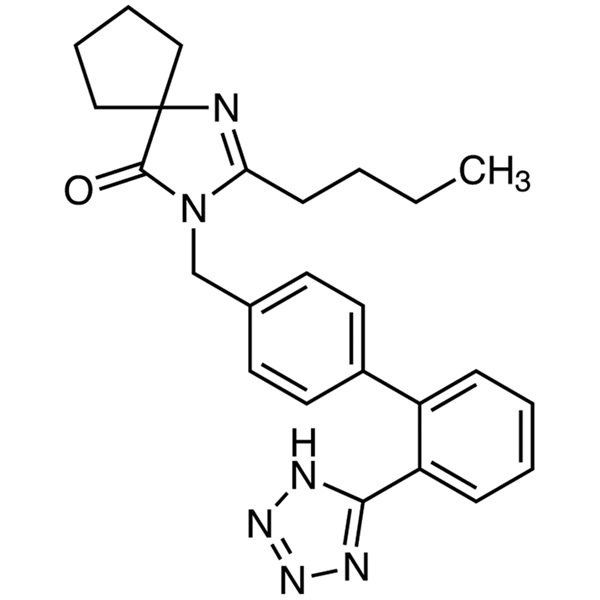
Irbesartan CAS 138402-11-6 Ensayo 98,0~102,0% (HPLC) API USP Estándar Antihipertensivo
Ruifu Chemical es el proveedor líder de Irbesartan (CAS: 138402-11-6) con alta calidad y puede cumplir con el estándar USP. Ruifu Chemical lleva más de 15 años suministrando API e intermedios farmacéuticos.
Ruifu Chemical puede ofrecer entregas en todo el mundo, precios competitivos y excelente servicio.
Comprar Irbesartan y productos intermedios relacionados, por favor contáctenos por correo electrónico: alvin@ruifuchem.com
| Nombre químico | Irbesartán |
| Sinónimos | BMS-186295; SR-47436; Aprovel; Avapro; 2-Butilo-3-[[2′-(1H-tetrazol-5-il)[1,1′-bifenil]-4-il]metil]-1,3-diazaspiro[4.4]non-1-en-4-ona; 2-Butil-3-[[4-[2-(2H-tetrazol-5-il)fenil]fenil]metil]-1,3-diazaspiro[4.4]non-1-en-4-ona |
| Número CAS | 138402-11-6 |
| Estado del stock | En stock, la producción aumenta hasta toneladas |
| Fórmula molecular | C25H28N6O |
| Peso Molecular | 428.54 |
| densidad | 1,30±0,10 g/cm3 |
| Punto de fusión | 184,0 a 188,0 ℃ |
| Solubilidad en agua | Insoluble en agua |
| COA y MSDS | Disponible |
| Temperatura de almacenamiento | Almacenar a largo plazo a 2-8 ℃ |
| Origen del producto | Shanghái, China |
| Categorías de productos | API (ingrediente farmacéutico activo) |
| Marca | Química Ruifu |
| Artículos de prueba | Especificaciones | Resultados |
| Apariencia | Polvo cristalino de color blanco a casi blanco. | Polvo cristalino blanco |
| Identificación | ||
| IR | Debe cumplir con el estándar de referencia. | Cumple |
| HPLC | Debe cumplir con el estándar de referencia. | Cumple |
| Contenido de agua (por K.F) | ≤0,50% | 0,15% |
| Ceniza Sulfatada | ≤0,20% | <0,20% |
| Carnes Pesadas | ≤0,002% | <0,002% |
| Límite de azida | ≤10 ppm | <10 ppm |
| Impurezas Orgánicas | ||
| Compuestos relacionados A de irbesartán | ≤0,20% | 0,002% |
| Cualquier otra impureza individual | ≤0,10% | 0,004% |
| Impurezas totales | ≤0,50% (Excluyendo R-Isómero) | 0,33% |
| Solventes residuales | ||
| etanol | ≤5000 ppm | 28 ppm |
| diclorometano | ≤600 ppm | No detectado |
| N,N-Dimetilformamida | ≤880 ppm | No detectado |
| t-Éter butílico metílico | ≤5000 ppm | No detectado |
| xileno | ≤1500 ppm | 320 ppm |
| tolueno | ≤890 ppm | No detectado |
| Ensayo (HPLC) | 98,0~102,0% de Irbesartan (C25H28N6O), calculado en base anhidra | 99,9% |
| Conclusión | El producto ha sido probado y cumple con la norma USP 36. | |
Paquete: Botella, bolsa de papel de aluminio, 25 kg/tambor de cartón, o según requerimiento del cliente.
Condición de almacenamiento: Mantener el recipiente bien cerrado. Almacenar en un lugar fresco, seco (2-8℃) y bien ventilado, lejos de sustancias incompatibles. Mantener alejado de la luz del sol; evitar el fuego y las fuentes de calor; evitar la humedad.
Envío: Entrega a todo el mundo por aire, mar, por FedEx / DHL Express. Proporcionar una entrega rápida y confiable.

Símbolos de peligro Xn - Nocivo
Códigos de riesgo 22 - Nocivo si se ingiere
Descripción de seguridad
S26 - En caso de contacto con los ojos, enjuagar inmediatamente con abundante agua y consultar a un médico.
S24/25 - Evite el contacto con la piel y los ojos.
WGK Alemania 3
RTECS HM2950270
Código SA 2933290090
Irbesartán (CAS: 138402-11-6) es un antagonista del receptor de angiotensina II utilizado principalmente para el tratamiento de la hipertensión. Irbesartán fue desarrollado por Sanofi Research (ahora parte de Sanofi-Aventis). Lo comercializan conjuntamente Sanofi (Aventis) y Bristol (Myers Squibb) bajo los nombres comerciales Aprovel, Karvea y Avapro. Irbesartan se usa para tratar la presión arterial alta. Avapro se lanzó en Alemania, el Reino Unido y los EE. UU. para la hipertensión. Como ocurre con todos los antagonistas de los receptores de angiotensina II, irbesartán está indicado para el tratamiento de la hipertensión.
Irbesartán también puede retrasar la progresión de la nefropatía diabética y también está indicado para reducir la progresión de la enfermedad renal en pacientes con diabetes tipo 2, hipertensión y microalbuminuria (>30 mg/24 horas) o proteinuria. Irbesartán también puede reducir la remodelación eléctrica del miocardio, reduciendo así la tasa de mortalidad de los pacientes con hipertensión; es el fármaco más eficaz para el tratamiento de la hipertensión y las enfermedades cardiovasculares.
Irbesartán
C25H28N6O 428,53
1,3-Diazaspiro[4.4]non-1-en-4-ona, 2-butil-3-[[2′-(1H-tetrazol-5-il)[1,1′-bifenil]-4-il]metil]-;
2-Butil-3-[p-(o-1H-tetrazol-5-ilfenil)bencil]-1,3-diazaspiro[4.4]non-1-en-4-ona [138402-11-6]; UNII: J0E2756Z7N.
DEFINICIÓN
Irbesartán contiene no menos de 98,0% y no más de 102,0% de irbesartán (C25H28N6O), calculado en base anhidra.
IDENTIFICACIÓN
Cambiar para leer:
• A. PRUEBAS DE IDENTIFICACIÓN ESPECTROSCÓPICA<197>, Espectroscopia Infrarroja: 197K (CN 1-MAYO-2020)
• B. El tiempo de retención del pico principal de la Solución muestra corresponde al de la Solución estándar, tal como se obtiene en la Valoración.
ENSAYO
• PROCEDIMIENTO
Tampón: Ácido fosfórico y agua (v/v) (5,5:950). Ajustar con trietilamina a un pH de 3,2.
Fase móvil: Acetonitrilo y Tampón (330:670)
Solución de idoneidad del sistema: 0,05 mg/mL de ER Irbesartán USP y ER Compuesto Relacionado A de Irbesartán USP en metanol
Solución estándar: 0,5 mg/mL de ER Irbesartán USP en metanol
Solución muestra: 0,5 mg/mL de Irbesartán en metanol
sistema cromatográfico
(Consulte Cromatografía<621>, Idoneidad del sistema).
Modo: LC
Detector: UV 220 nm
Columna: 4,0-mm × 25-cm; embalaje L1
Caudal: 1 ml/min
Volumen de inyección: 10 µL
Idoneidad del sistema
Muestras: Solución de idoneidad del sistema y Solución estándar
[ NOTA- Los tiempos de retención relativos para el compuesto relacionado A de irbesartán y para irbesartán son 0,8 y 1,0, respectivamente.]
Requisitos de idoneidad
Resolución: No menos de 2,0 entre irbesartán y compuesto relacionado A de irbesartán, Solución de idoneidad del sistema
Desviación estándar relativa: No más de 1,0%, Solución estándar
Análisis
Muestras: Solución estándar y Solución muestra
Calcule el porcentaje de irbesartán (C25H28N6O) en la porción de Irbesartán tomada:
Resultado = (ru /rs ) × (Cs /Cu) × 100
ru = respuesta máxima de Irbesartán de la Solución muestra
rs = respuesta máxima de Irbesartán de la Solución estándar
Cs = concentración de ER Irbesartán USP en la Solución estándar (mg/mL)
Cu = concentración de Irbesartán en la Solución muestra (mg/mL)
Criterios de aceptación: 98,0%-102,0% en base anhidra
IMPUREZAS
• LÍMITE DE AZIDA
Fase móvil: solución de hidróxido de sodio 0,1 N
Solución madre estándar: 0,25 mg/mL de azida sódica en fase móvil
Solución estándar: 0,312 µg/mL de azida sódica en Fase móvil, de la Solución madre del estándar
Solución muestra: 20 mg/mL de Irbesartán en Fase móvil
sistema cromatográfico
(Consulte Cromatografía<621>, Idoneidad del sistema).
Modo: LC
Detector: Conductimétrico con una unidad supresora de fondo adecuada
Columna: 4,0-mm × 25-cm; embalaje L31
Caudal: 1 ml/min
Volumen de inyección: 200 µL
Idoneidad del sistema
Muestra: Solución estándar
Requisitos de idoneidad
Relación señal-ruido: no menos de 10 para el pico de azida
Análisis
Muestras: Solución estándar y Solución muestra
Calcule la cantidad de azida, en ppm, en la porción de Irbesartán tomada:
Resultado = (ru /rs) × (Cs/Cu) × (Mr1 /Mr2) × F
ru = área del pico de azida de la Solución muestra
rs = área del pico de azida de la Solución estándar
Cs = concentración de azida sódica en la Solución estándar (µg/mL)
Cu = concentración de Irbesartán en la Solución muestra (mg/mL)
Mr1 = peso molecular de la azida, 42,02
Mr2 = peso molecular de la azida sódica, 65,01
F = factor de conversión de unidades, 1000
Criterios de aceptación: No más de 10 ppm
• IMPUREZAS ORGÁNICAS
Tampón y fase móvil: preparar según se indica en el ensayo.
Solución estándar: Utilice la solución de idoneidad del sistema, preparada según las indicaciones del Análisis.
Solución muestra: 1 mg/mL de Irbesartán en metanol
sistema cromatográfico
(Consulte Cromatografía<621>, Idoneidad del sistema).
Modo: LC
Detector: UV 220 nm
Columna: 4,0-mm × 25-cm; embalaje L1
Caudal: 1 ml/min
Volumen de inyección: 10 µL
Idoneidad del sistema
Muestra: Solución estándar
Requisitos de idoneidad
Desviación estándar relativa: no más de 2,0%
Análisis
Muestras: Solución estándar y Solución muestra
Calcule el porcentaje del compuesto relacionado A de irbesartán en la porción de Irbesartán tomada:
Resultado = (ru /rs ) × (Cs /Cu ) × 100
ru = respuesta máxima del compuesto relacionado A de irbesartán de la Solución muestra
rs = respuesta máxima del compuesto relacionado A de irbesartán de la Solución estándar
Cs = concentración de ER Compuesto Relacionado A de Irbesartán USP en la Solución estándar (mg/mL)
Cu = concentración de Irbesartán en la Solución muestra (mg/mL)
Calcule el porcentaje de cualquier otra impureza en la porción de Irbesartán tomada:
Resultado = (ru /rs ) × (Cs /Cu ) × 100
ru = respuesta máxima de cualquier otra impureza de la Solución muestra
rs = respuesta máxima de Irbesartán de la Solución estándar
Cs = concentración de ER Irbesartán USP en la Solución estándar (mg/mL)
Cu = concentración de Irbesartán en la Solución muestra (mg/mL)
Criterios de aceptación
Compuesto relacionado A de irbesartán: no más de 0,2%
Cualquier otra impureza: no más de 0,1%
Impurezas totales: no más de 0,5%
PRUEBAS ESPECÍFICAS
• DETERMINACIÓN DEL AGUA, Método I<921>: No más de 0,5%
REQUISITOS ADICIONALES
• ENVASADO Y ALMACENAMIENTO: Conservar en recipientes herméticos y almacenar a temperatura inferior a 30°.
• ESTÁNDARES DE REFERENCIA USP<11>
Irbesartán ER USP
ER Compuesto Relacionado A de Irbesartán USP
1-Pentanoilamino-ácido ciclopentanocarboxílico [2′-(1H-tetrazol-5-il)-bifenil-4-ilmetil]-amida.
C25H30N6O 446,54