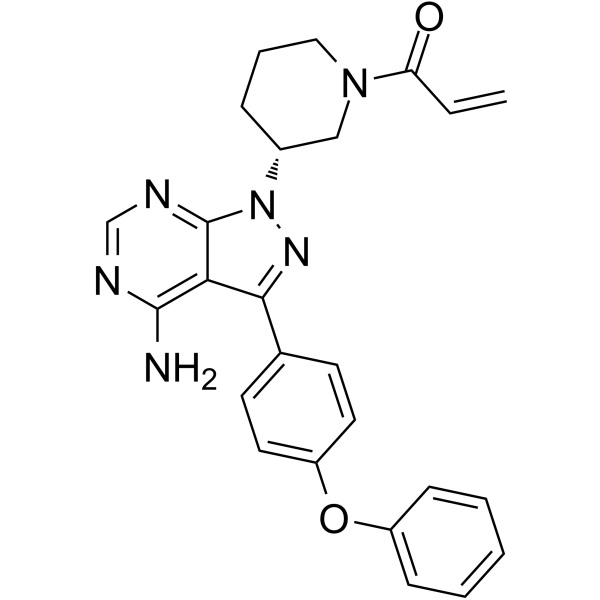
Ibrutinib CAS 936563-96-1 Pureza >99,5% (HPLC) API
| Nombre químico | Ibrutinib |
| Sinónimos | 1-[(3R)-3-[4-Amino-3-(4-fenoxifenil)-1H-pirazolo[3,4-d]pirimidin-1-il]-1-piperidinil]-2-propen-1-ona; PCI-32765 |
| Número CAS | 936563-96-1 |
| Estado del stock | En stock, la producción aumenta hasta toneladas |
| Fórmula molecular | C25H24N6O2 |
| Peso Molecular | 440.50 |
| COA y MSDS | Disponible |
| Origen | Shanghái, China |
| Marca | Química Ruifu |
| Artículo | Especificaciones |
| Apariencia | Blanco a blanquecino - Polvo de cristal |
| Identificación | RI; HPLC |
| Pérdida por secado | <0,50% |
| Residuo en el encendido | ≤0,10% |
| Metales pesados (como Pb) | ≤20 ppm |
| Cualquier impureza única | ≤0,50% |
| Impurezas totales | <0,50% |
| Método de pureza/análisis | >99,5% (HPLC) |
| Estándar de prueba | Estándar empresarial |
| Uso | API |
Paquete: Botella, Bolsa de papel de aluminio, 25kg/Bidón de cartón, o según requerimiento del cliente.
Condición de almacenamiento:Almacenar en recipientes sellados en lugar fresco y seco; Proteger de la luz y la humedad.

Ibrutinib (CAS: 936563-96-1) es un inhibidor de la tirosina quinasa de Bruton (BTK) para el tratamiento de la leucemia linfocítica crónica (LLC) y el linfoma de células del manto (MCL). Tanto el MCL como el CLL pertenecen al linfoma no Hodgkin de células B, que es refractario y propenso a recaer. La quimioinmunoterapia comúnmente utilizada no tiene un objetivo específico y a menudo ocurren reacciones adversas de grado 3 o 4. Ibrutinib puede combinarse con BTK, que es necesaria para la formación, diferenciación, comunicación y supervivencia de los linfocitos B, e inhibir irreversiblemente la actividad de BTK, inhibir eficazmente la proliferación y supervivencia de las células tumorales. Además, se absorbe rápidamente después de la administración oral, la concentración plasmática máxima se alcanza entre 1 y 2 horas y las reacciones adversas son de grado 1 o 2, lo que se convertirá en una nueva opción para el tratamiento de CLL y MCL. El 13 de noviembre de 2013, la FDA de EE. UU. aceleró la aprobación de la compañía Johnson & Johnson y de Estados Unidos Imbruvica (nombre común: Ibrutinib) para el tratamiento del linfoma de células del manto (MCL). La FDA otorgó a ibrutinib el estado de terapia innovadora en febrero de 2013 y fue aprobado para MCL el 13 de noviembre de 2013 y CLL el 12 de febrero de 2014, respectivamente.