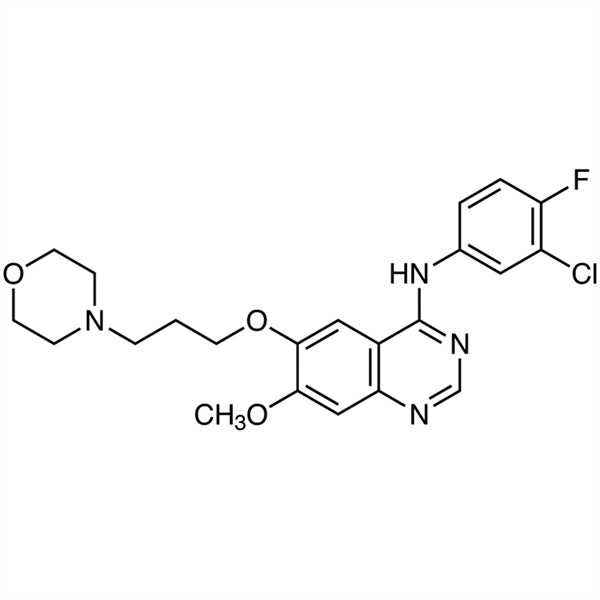
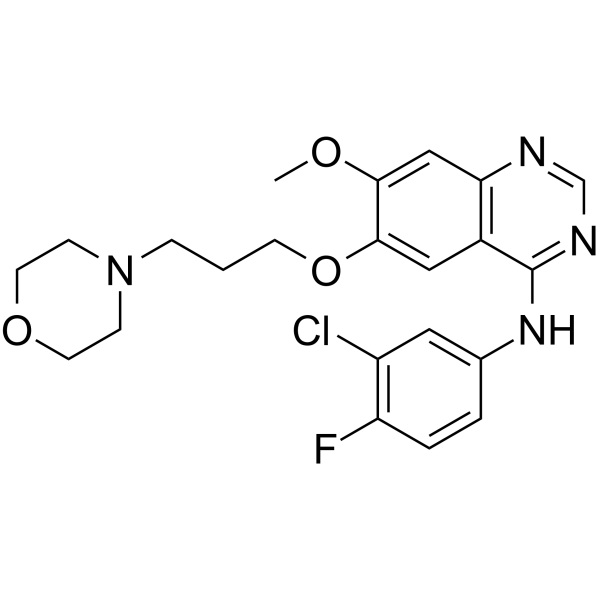
Gefitinib CAS 184475-35-2 Pureza >99,5% (HPLC)
Shanghai Ruifu Chemical Co., Ltd. es el fabricante líder de Gefitinib (CAS: 184475-35-2) de alta calidad. Ruifu Chemical puede ofrecer entregas en todo el mundo, precios competitivos, excelente servicio y cantidades pequeñas y al por mayor disponibles. Compra Gefitinib y productos intermedios, Por favor contacte: alvin@ruifuchem.com
| Nombre químico | Gefitinib |
| Sinónimos | Base libre de gefitinib; Iressa; ZD1839; ZD-1839; N-(3-Cloro-4-Fluorofenil)-7-Metoxi-6-(3-Morfolinopropoxi)quinazolin-4-Amina; N-(3-Cloro-4-Fluorofenil)-7-Metoxi-6-[3-(4-Morfolinil)propoxi]-4-Quinazolinamina |
| Estado del stock | En stock, producción comercial |
| Número CAS | 184475-35-2 |
| Fórmula molecular | C22H24ClFN4O3 |
| Peso Molecular | 446,91 g/mol |
| Punto de fusión | 194,0 a 198,0 ℃ |
| densidad | 1,322±0,06g/cm3 |
| Solubilidad | Insoluble en agua. Soluble en DMSO |
| Temperatura de almacenamiento. | Temperatura ambiente |
| Envío | ambiente |
| COA y MSDS | Disponible |
| Origen | Shanghái, China |
| Categorías de productos | API (ingrediente farmacéutico activo) |
| Marca | Química Ruifu |
| Artículos | Estándares de inspección | Resultados |
| Apariencia | Blanco a blanquecino en polvo | Cumple |
| Pérdida por secado | <0,50% | 0,13% |
| Residuo en el encendido | <0,20% | 0,06% |
| Impureza única | <0,10% | 0,09% |
| Impurezas totales | <0,50% | 0,20% |
| Metales pesados (Pb) | ≤10 ppm | <10 ppm |
| Pureza de gefitinib | >99,5% (HPLC) | 99,80% |
| Espectro infrarrojo | Consistente con la estructura | Cumple |
| Espectro de RMN 1H | Consistente con la estructura | Cumple |
| Conclusión | El producto ha sido probado y cumple con las especificaciones dadas. | |
Paquete: Botella de Fluorado, Bolsa de papel de aluminio, 25kg/Bidón de Cartón, o según requerimiento del cliente.
Condición de almacenamiento: Mantener el recipiente bien cerrado y almacenar en un lugar fresco, seco y bien ventilado, lejos de sustancias incompatibles. Proteger de la luz y la humedad.
Envío:Entrega a todo el mundo por vía aérea, por FedEx / DHL Express. Proporcionar una entrega rápida y confiable.
No apto para uso en humanos. No apto para uso diagnóstico o terapéutico. Sólo para uso en investigación in vitro.
Ninguno de los productos se suministrará a países en los que esto pueda entrar en conflicto con las patentes existentes. Sin embargo, la responsabilidad final recae en el Comprador.
¿Cómo comprar? Por favor contacteDr. Alvin Huang: sales@ruifuchem.com o alvin@ruifuchem.com
¿15 años de experiencia?Contamos con más de 15 años de experiencia en la fabricación y exportación de una amplia gama de productos químicos finos o intermedios farmacéuticos de alta calidad.
¿Principales mercados? Vender al mercado interno, América del Norte, Europa, India, Corea, Japón, Australia, etc.
¿Ventajas? Calidad superior, precio asequible, servicios profesionales y soporte técnico, entrega rápida.
Calidad Aseguramiento? Estricto sistema de control de calidad. Los equipos profesionales para análisis incluyen NMR, LC-MS, GC, HPLC, ICP-MS, UV, IR, OR, K.F, ROI, LOD, MP, claridad, solubilidad, prueba de límite microbiano, etc.
Muestras? La mayoría de los productos proporcionan muestras gratuitas para la evaluación de la calidad; el costo de envío debe ser pagado por los clientes.
Auditoría de fábrica? Bienvenida a la auditoría de fábrica. Por favor programe una cita con anticipación.
¿MOQ? Sin cantidad mínima de pedido. Se aceptan pedidos pequeños.
Tiempo de entrega? Si hay stock, entrega en tres días garantizada.
Transporte? Por expreso (FedEx, DHL), por aire, por mar.
¿Documentos? Servicio posventa: se pueden proporcionar COA, MOA, ROS, MSDS, etc.
Síntesis personalizada? Puede proporcionar servicios de síntesis personalizados que se adapten mejor a sus necesidades de investigación.
Condiciones de pago? La factura proforma se enviará primero después de la confirmación del pedido, adjuntando nuestros datos bancarios. Pago por T/T (Transferencia Télex), PayPal, Western Union, etc.
| Descripción de seguridad | 24/25 - Evite el contacto con la piel y los ojos. |
| Código HS | 2934999099 |
Gefitinib (CAS: 184475-35-2) es un fármaco terapéutico antitumoral altamente específico desarrollado por AstraZeneca, Reino Unido. Es el primer fármaco dirigido molecularmente para el tratamiento del cáncer de pulmón de células no pequeñas. Actúa inhibiendo selectivamente la vía de transducción de señales de la tirosina quinasa del receptor del factor de crecimiento epidérmico (EGFR-TK). El factor de crecimiento epidérmico (EGF) es un polipéptido con una masa molecular relativa de 6,45 × 103, que puede combinarse con el receptor del factor de crecimiento epidérmico (EGFR) en la membrana de la célula diana para producir efectos biológicos. EGFR es un receptor de tipo tirosina quinasa (TK). Cuando se une al EGF, puede promover la activación de TK en el cuerpo receptor, lo que resulta en la autofosforilación de los residuos de tirosina del receptor, proporcionando señales de división continua a las células, lo que provoca la proliferación y diferenciación celular. EGFR es abundante en los tejidos humanos y se expresa altamente en tumores malignos. Al bloquear la vía de señalización de EGFR en la superficie celular, gefitinib dificulta el crecimiento tumoral, la metástasis y la angiogénesis, y puede inducir la apoptosis de las células tumorales. En agosto de 2002, gefitinib se comercializó por primera vez en Japón como tratamiento de primera línea para el cáncer de pulmón de células no pequeñas con el nombre comercial Iressa. En mayo de 2003, la Administración de Alimentos y Medicamentos de EE. UU. aprobó el gefitinib como monoterapia de tercera línea para pacientes con cáncer de pulmón de células no pequeñas avanzado que resultaron ineficaces con medicamentos anticancerígenos a base de platino y quimioterapia con docetaxel. Actualmente, ha sido aprobado por Australia, Japón, Argentina, Singapur y Corea del Sur para el tratamiento del cáncer de pulmón de células no pequeñas avanzado. El 28 de febrero de 2005, la Administración de Alimentos y Medicamentos de China aprobó gefitinib para el tratamiento del cáncer de pulmón de células no pequeñas (CPCNP) localmente avanzado o metastásico que había recibido quimioterapia previamente. Actualmente no está aprobado para su uso como terapia de primera línea para el NSCLC avanzado. El 1 de julio de 2009, la Agencia Europea de Medicamentos aprobó oficialmente gefitinib para el tratamiento de primera, segunda y tercera línea del cáncer de pulmón de células no pequeñas localmente avanzado o metastásico con mutaciones del gen EGFR en adultos.