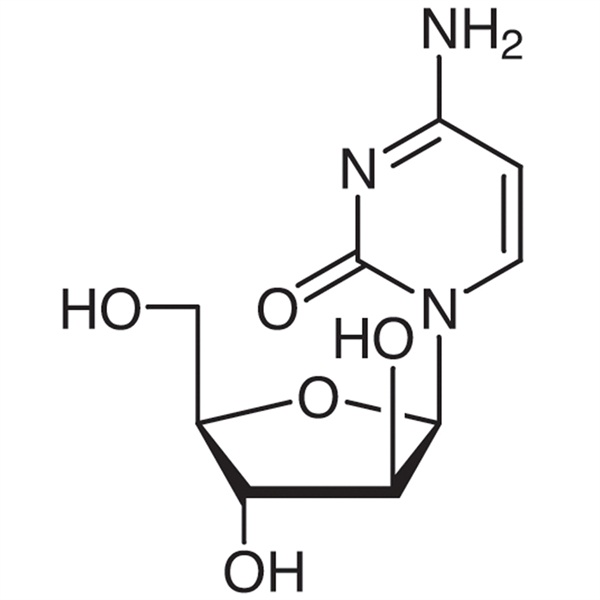
Citarabina (Ara-C) CAS 147-94-4 Ensayo 98,0%~102,0% Alta calidad de fábrica
Shanghai Ruifu Chemical Co., Ltd. es el fabricante líder de citarabina (Ara-C) (CAS: 147-94-4) con alta calidad. Ruifu Chemical puede ofrecer entregas en todo el mundo, precios competitivos, excelente servicio y cantidades pequeñas y al por mayor disponibles. Comprar citarabina, Por favor contacte: alvin@ruifuchem.com
| Nombre químico | citarabina |
| Sinónimos | Ara-C; arabinocitidina; Citosina β-D-Arabinofuranósido; arabinofuranosilcitosina; 4-Amino-1-β-D-Arabinofuranosil-2(1H)-Pirimidinona |
| Número CAS | 147-94-4 |
| Estado del stock | En stock, producción comercial |
| Fórmula molecular | C9H13N3O5 |
| Peso Molecular | 243.22 |
| Punto de fusión | 214℃ |
| Solubilidad en agua | Soluble en agua |
| COA y MSDS | Disponible |
| Origen del producto | China |
| Marca | Química Ruifu |
| Artículo | Especificaciones | Resultados |
| Apariencia | Polvo cristalino blanco | Polvo cristalino blanco |
| Solubilidad | Totalmente soluble en agua, muy ligeramente soluble en Alcohol y cloruro de metileno. | Cumple |
| Identificación A | IR Conforme a RS | Cumple |
| Identificación B | Rf se ajusta a RS (HPLC) | Cumple |
| Rotación específica | +154,0°~+160,0° | +158,1° |
| Pérdida por secado | ≤1,00% | 0,67% |
| Residuo en el encendido | ≤0,50% | 0,08% |
| Metales pesados | ≤10 ppm | <10 ppm |
| Impureza cromatográfica | ||
| Impurezas totales | ≤0,30% (HPLC) | 0,23% |
| uridina | ≤0,10% (HPLC) | <0,10% |
| uracilo | ≤0,10% (HPLC) | <0,10% |
| Arabinofuranosiluracilo | ≤0,30% (HPLC) | <0,30% |
| Ensayo | 98,0% ~102,0% | 99,70% |
| Estándar de prueba | Cumple con USP41 | Cumple |
Paquete: Botella, bolsa de papel de aluminio, tambor de cartón de 25 kg o según los requisitos del cliente.
Condición de almacenamiento: Mantener el recipiente bien cerrado y almacenar en un lugar fresco, seco y bien ventilado, lejos de sustancias incompatibles. Mantener alejado de la luz del sol; evitar el fuego y las fuentes de calor; evitar la humedad.
Envío: Entrega a todo el mundo por aire, mar, por FedEx / DHL Express. Proporcionar una entrega rápida y confiable.
citarabina
C9H13N3O5 243,22
2(1H)-pirimidinona, 4-amino-1--d-arabinofuranosilo-.
1--d-Arabinofuranosilcitosina [147-94-4].
» La citarabina contiene no menos del 98,0 por ciento y no más del 102,0 por ciento de C9H13N3O5, calculado sobre la base seca.
Embalaje y almacenamiento- Conservar en recipientes bien cerrados y resistentes a la luz.
Etiquetado- Cuando está destinado a usarse en la preparación de formas de dosificación inyectables, la etiqueta indica que es estéril o que debe someterse a un procesamiento adicional durante la preparación de formas de dosificación inyectables.
Estándares de referencia USP<11>-
ER Citarabina USP
ER Endotoxina USP
ER Uracilo Arabinósido USP
Identificación-
A: Absorción Infrarroja<197M>: previamente secado a una presión no mayor a 5 mm de mercurio a 60ºC durante 3 horas.
B: El tiempo de retención del pico principal en el cromatograma de la Preparación de ensayo corresponde al del cromatograma de la Preparación estándar, tal como se obtiene en el Ensayo.
Rotación específica<781S>: entre +154 y +160.
Solución de prueba: 10 mg por ml, en agua.
Pérdida por secado<731>- Secarlo al vacío a una presión no superior a 5 mm de mercurio a 60ºC durante 3 horas: no pierde más del 1,0% de su peso.
Residuo por ignición<281>: no más del 0,5%.
Metales pesados, Método II<231>: 0,001%.
Pureza cromatográfica-
Tampón de fosfato- Prepare una solución que contenga fosfato de sodio monobásico 0,01 M y fosfato de sodio dibásico 0,01 M en un recipiente adecuado. Ajustar con hidróxido de sodio 0,1 M o ácido fosfórico 0,1 M a un pH de 7,0.
Solución A- Preparar una mezcla filtrada y desgasificada de tampón fosfato y metanol (49:1). Realice ajustes si es necesario (consulte Idoneidad del sistema en Cromatografía<621>). Prepare esta solución fresca todos los días.
Solución B- Preparar una mezcla filtrada y desgasificada de tampón fosfato y metanol (7:3). Realice ajustes si es necesario (consulte Idoneidad del sistema en Cromatografía<621>). Prepare esta solución fresca todos los días.
Fase móvil- Utilice mezclas variables de Solución A y Solución B como se indica en Sistema cromatográfico.
Solución de idoneidad del sistema- Disuelva cantidades adecuadas de uridina, ER Uracilo Arabinósido USP y ER Citarabina USP en agua para obtener una solución que contenga aproximadamente 0,02, 0,02 y 5,0 mg por ml, respectivamente.
Solución estándar- Disolver una cantidad pesada con precisión de ER Citarabina USP en agua y diluir cuantitativamente, y gradualmente si es necesario, con agua para obtener una solución que tenga una concentración conocida de aproximadamente 4 µg por ml.
Solución de prueba- Transfiera aproximadamente 25 mg de citarabina, pesados con precisión, a un matraz aforado de 5,0 ml, disuélvalos y diluya a volumen con agua y mezcle. [nota-Prepare esta solución fresca todos los días.]
Sistema cromatográfico (ver Cromatografía<621>)-El cromatógrafo líquido está equipado con un detector de 254-nm y una columna de 4,6-mm × 25-cm que contiene el relleno L1. El caudal es de aproximadamente 1 ml por minuto. El cromatógrafo está programado para proporcionar mezclas variables de Solución A y Solución B, siendo el porcentaje de Solución B 0% en el momento de la inyección. Esta composición se mantiene durante 10 minutos. Luego se aumenta linealmente la solución B hasta el 100% durante un período de 10 minutos. Después de mantener esta composición durante 5 minutos, el porcentaje de Solución B se reduce linealmente al 0% durante un período de 5 minutos. Esta composición se mantiene durante 20 minutos para equilibrar el sistema. Cromatografía la solución de idoneidad del sistema y registra las respuestas de los picos como se indica en Procedimiento: los tiempos de retención relativos son aproximadamente 0,55 para uracilo, 1,14 para uridina, 1,62 para uracilo arabinósido y 1,0 para citarabina; y la resolución, R, entre citarabina y uridina no es inferior a 1,25. Cromatografía la solución estándar y registra las respuestas de los picos como se indica en Procedimiento: la desviación estándar relativa para inyecciones repetidas no es superior al 3,0 %.
Procedimiento- Inyecte volúmenes iguales (aproximadamente 20 µL) de la Solución estándar y la Solución de prueba en el cromatógrafo, registre los cromatogramas y mida las respuestas de los picos. Calcule el porcentaje de arabinósido de uracilo en la porción de citarabina tomada mediante la fórmula:
500(C/W)(ri/1,34rS)
en la que C es la concentración, en mg por ml, de ER Citarabina USP en la Solución estándar; W es el peso, en mg, de la muestra, 1,34 es el factor de respuesta relativa para el uracilo arabinósido; ri es la respuesta máxima del arabinósido de uracilo en la solución de prueba; y rS es la respuesta máxima de Citarabina ER USP en la Solución estándar: no se encuentra más del 0,30 %.
Calcule el porcentaje de todas las demás impurezas en la porción de citarabina tomada mediante la fórmula:
500(C/W)(ri/FrS)
en la que C es la concentración, en mg por ml, de ER Citarabina USP en la Solución estándar; W es el peso, en mg, de la muestra; ri es la respuesta máxima de cada impureza en la solución de prueba; rS es la respuesta máxima de Citarabina ER USP en la Solución estándar; y F, el factor de respuesta relativa, es igual a 2,5 para el pico de uracilo, con un tiempo de retención relativo de 0,55, 1,5 para picos con tiempos de retención relativos de 0,38, 0,43 y 1,14, y 1,0 para todos los demás picos. No se encuentra más del 0,10 % de cualquier impureza individual y no más del 0,30 % del total de impurezas (incluido el uracilo arabinósido).
Otros requisitos- Cuando la etiqueta indica que citarabina es estéril, cumple con los requisitos de las pruebas de esterilidad 71 y de endotoxinas bacterianas en citarabina inyectable. Cuando la etiqueta indica que la citarabina debe someterse a un procesamiento adicional durante la preparación de formas farmacéuticas inyectables, cumple con los requisitos para endotoxinas bacterianas bajo citarabina para inyección.
Ensayo-
Tampón de fosfato- Disolver 0,73 g de fosfato de sodio monobásico y 1,4 g de fosfato de sodio dibásico en 1 litro de agua, mezclar y filtrar.
Fase móvil- Preparar una mezcla filtrada y desgasificada de tampón fosfato y metanol (95:5). Realice ajustes si es necesario (consulte Idoneidad del sistema en Cromatografía<621>).
Preparación estándar- Disolver una cantidad pesada con precisión de ER Citarabina USP en agua y diluir cuantitativamente, y gradualmente si es necesario, con agua para obtener una solución que tenga una concentración conocida de aproximadamente 0,1 mg por ml.
Solución de resolución- Disolver una cantidad pesada con precisión de ER Uracilo Arabinósido USP en la Preparación estándar y diluir cuantitativamente, y gradualmente si es necesario, con la Preparación estándar para obtener una solución que tenga una concentración conocida de aproximadamente 0,1 mg por ml.
Preparación del ensayo- Transfiera aproximadamente 10 mg de citarabina, pesados con precisión, a un matraz aforado de 100 ml, disuélvalos y diluya a volumen con agua y mezcle.
Sistema cromatográfico (ver Cromatografía<621>)-El cromatógrafo líquido está equipado con un detector de 254-nm y una columna de 4,6-mm × 25-cm que contiene el relleno L1. El caudal es de aproximadamente 1,0 ml por minuto. Cromatografía la solución de resolución y registra las respuestas de los picos como se indica en el Procedimiento: los tiempos de retención relativos son aproximadamente 1,0 para citarabina y 1,3 para uracilo arabinósido; y la resolución, R, entre citarabina y uracilo arabinósido no es inferior a 2,5. Cromatografía la preparación estándar y registra las respuestas máximas como se indica en el Procedimiento: la desviación estándar relativa para inyecciones repetidas no es superior al 2,0 %. [nota-Una vez completada la cromatografía, enjuague la columna con una mezcla de agua y metanol (7:3).]
Procedimiento- Inyecte por separado volúmenes iguales (aproximadamente 10 µL) de la preparación estándar y de la preparación de ensayo en el cromatógrafo, registre los cromatogramas y mida las respuestas de los picos principales. Calcule la cantidad, en mg, de C9H13N3O5 en la porción de citarabina tomada mediante la fórmula:
100C(ru/rS)
en la que C es la concentración, en mg por ml, de ER Citarabina USP en la Preparación estándar; y rU y rS son las respuestas máximas obtenidas de la preparación de ensayo y la preparación estándar, respectivamente.

Códigos de riesgo R43 - Puede provocar sensibilización por contacto con la piel.
R63 - Posible riesgo de daño al feto
R36/37/38 - Irrita los ojos, el sistema respiratorio y la piel.
R20/21/22 - Nocivo por inhalación, en contacto con la piel y por ingestión.
Descripción de seguridad S36/37 - Utilice ropa y guantes de protección adecuados.
S37/39 - Úsense guantes adecuados y protección para los ojos y la cara.
S36 - Utilice ropa protectora adecuada.
S26 - En caso de contacto con los ojos, enjuagar inmediatamente con abundante agua y consultar a un médico.
WGK Alemania 3
RTEC HA5425000
MARCA FLUKA F CÓDIGOS 10-23
Código SA 2934999099
Citarabina (CAS: 147-94-4) es un tipo de síntesis química antiviral de clase nucleósido de purina que inicialmente se extrajo del medio de streptomyces y luego se produjo a partir de síntesis química. Es un polvo cristalino blanco y muy ligeramente soluble en agua. Su éster monofosfato es fácilmente soluble en agua. Tiene efecto inhibidor sobre varios tipos de virus ADN, como el virus del herpes simple HSV1 y HSV2, el virus de la hepatitis B, el virus varicela-zoster y el citomegalovirus. Citarabina (CAS: 147-94-4), un agente de quimioterapia utilizado principalmente en el tratamiento de cánceres de glóbulos blancos como la leucemia mieloide aguda (LMA) y el linfoma no Hodgkin. La citarabina es un análogo de la citosina y un agente antineoplásico que se utiliza principalmente en el tratamiento de la leucemia aguda. La citarabina se asocia con una tasa baja de elevaciones transitorias de enzimas séricas y bilirrubina durante el tratamiento, pero rara vez se la ha implicado en casos de lesión hepática aguda clínicamente aparente con ictericia.