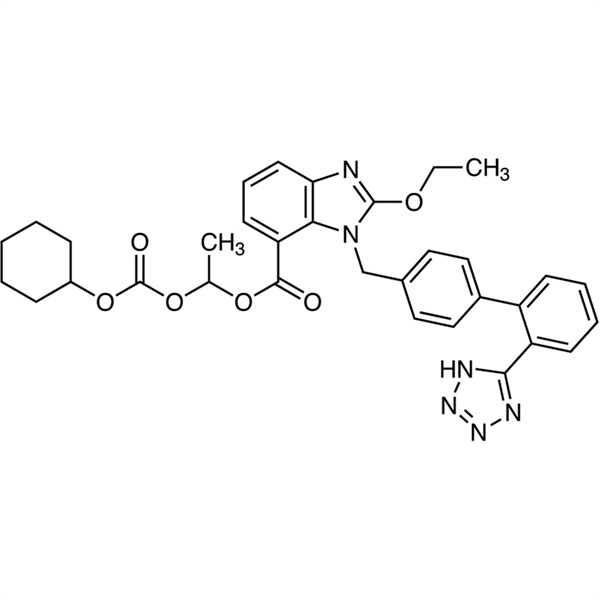
Candesartan Cilexetil CAS 145040-37-5 Ensayo 99,0~101,0% API EP estándar
Ruifu Chemical es el proveedor líder de candesartán cilexetilo (CAS: 145040-37-5) de alta calidad que puede cumplir con el estándar EP. Ruifu lleva más de 15 años suministrando API e intermedios farmacéuticos.
Ruifu Chemical puede ofrecer entregas en todo el mundo, precios competitivos y excelente servicio.
Compre Candesartan Cilexetil y sus intermedios, contáctenos por correo electrónico: alvin@ruifuchem.com
Intermedio de Candesartan Cilexetil del suministro químico de Ruifu con pureza elevada
Candesartán cilexetilo CAS 145040-37-5
Candesartán CAS 139481-59-7
1-Carbonato de cloroetilo ciclohexilo CAS 99464-83-2
Candesartán Cilexetil Éster etílico intermedio C6 CAS 139481-41-7
Candesartán Cilexetil Intermedio CAS 139481-44-0
Tritil candesartán cilexetilo CAS 170791-09-0
| Nombre químico | Candesartán Cilexetilo |
| Sinónimos | TCV-116; 1-(((Ciclohexiloxi)carbonil)oxi)etilo 1-((2'-(1H-tetrazol-5-il)-[1,1'-bifenil]-4-il)metil)-2-etoxi-1H-benzo[d]imidazol-7-Carboxilato |
| Número CAS | 145040-37-5 |
| Estado del stock | En stock, la producción aumenta hasta toneladas |
| Fórmula molecular | C33H34N6O6 |
| Peso Molecular | 610.66 |
| densidad | 1,37±0,10g/cm3 |
| Punto de fusión | 168,0-170,0℃ |
| COA y MSDS | Disponible |
| Condición de almacenamiento | 2-8℃ |
| sensible | Sensible al calor |
| Origen del producto | Shanghái, China |
| Categorías de productos | API (ingrediente farmacéutico activo) |
| Marca | Química Ruifu |
| Artículos | Especificaciones | Resultados |
| Apariencia | Polvo blanco o casi blanco | polvo blanco |
| Identificación-IR | Cumplir con el espectro de referencia. | Cumple |
| Identificación- ultravioleta | Absorciones máximas a 254 nm, absorción mínima a 242 nm | Cumple |
| Agua (K.F) | ≤0,30% | 0,19% |
| Solventes residuales | ||
| Metanol | ≤3000 ppm | No detectado |
| etanol | ≤5000 ppm | No detectado |
| Éter etílico | ≤5000 ppm | 62 ppm |
| acetona | ≤5000 ppm | 505 ppm |
| Acetato de etilo | ≤5000 ppm | No detectado |
| diclorometano | ≤600 ppm | No detectado |
| Dimetilformamida | ≤880 ppm | No detectado |
| Sustancias relacionadas | ||
| Impureza A | ≤0,15% | 0,04% |
| Impureza B | ≤0,30% | 0,03% |
| Impureza F | ≤0,20% | 0,02% |
| Impureza G | ≤0,20% | 0,04% |
| Impureza H | ≤0,15% | No detectado |
| Otra impureza individual | ≤0,10% | 0,04% |
| Impurezas totales | ≤0,60% | 0,23% |
| Ceniza Sulfatada | ≤0,10% | 0,07% |
| Metales pesados | ≤10 ppm | <10 ppm |
| Ensayo (sustancia seca) | 99,0~101,0% | 99,9% |
| Estándar de prueba | Estándar EP | Cumple |
Paquete: Botella, bolsa de papel de aluminio, 25 kg/tambor de cartón, o según requerimiento del cliente.
Condición de almacenamiento: Mantener el recipiente bien cerrado. Almacenar en un lugar fresco, seco (2-8℃) y bien ventilado, lejos de sustancias incompatibles. Mantener alejado de la luz del sol; evitar el fuego y las fuentes de calor; evitar la humedad.
Envío: Entrega a todo el mundo por aire, mar, por FedEx / DHL Express. Proporcionar una entrega rápida y confiable.

Códigos de riesgo
R20/21/22 - Nocivo por inhalación, en contacto con la piel y por ingestión.
R36/37/38 - Irrita los ojos, el sistema respiratorio y la piel.
R50 - Muy tóxico para los organismos acuáticos.
R48/20 -
R61 - Puede causar daño al feto
Descripción de seguridad
S26 - En caso de contacto con los ojos, enjuagar inmediatamente con abundante agua y consultar a un médico.
S36 - Utilice ropa protectora adecuada.
S61 - Evite su liberación al medio ambiente. Consulte las instrucciones especiales/fichas de datos de seguridad.
S45 - En caso de accidente o malestar, acuda inmediatamente al médico (si es posible, muéstrele la etiqueta).
S53 - Evite la exposición - Obtenga instrucciones especiales antes de su uso.
WGK Alemania 3
RTECS DD6672500
Código SA 2933990099
Candesartán Cilexetil (TCV-116) (CAS: 145040-37-5) es un antagonista del receptor de angiotensina II con una CI50 de 0,26 nM, utilizado en el tratamiento de la hipertensión. Candesartán es un bloqueador de los receptores de angiotensina (BRA) que puede usarse solo o con otros agentes para tratar la hipertensión. Se administra por vía oral como profármaco, candesartán cilexetilo, que se convierte rápidamente en su metabolito activo, candesartán, durante la absorción en el tracto gastrointestinal. Candesartán reduce la presión arterial al antagonizar el sistema renina-angiotensina-aldosterona (SRAA); compite con la angiotensina II por unirse al subtipo del receptor de angiotensina II tipo 1 (AT1) y previene los efectos de la angiotensina II que aumentan la presión arterial. A diferencia de los inhibidores de la enzima convertidora de angiotensina (ECA), los BRA no tienen el efecto adverso de la tos seca. Candesartán puede usarse para tratar la hipertensión, la hipertensión sistólica aislada, la hipertrofia ventricular izquierda y la nefropatía diabética. También puede utilizarse como agente alternativo para el tratamiento de la insuficiencia cardíaca, la disfunción sistólica, el infarto de miocardio y la enfermedad de las arterias coronarias.
CANDESARTÁN CILEXETIL
Candesartanum cilexetili
C33H34N6O6 Señor 611
[145040-37-5]
DEFINICIÓN
(1RS)-1-[[(Ciclohexiloxi)carbonil]oxi]etilo
2-etoxi-1-[[2′-(1H-tetrazol-5-il)bifenil-4-il]metil]-1H-bencimidazol-7-carboxilato.
Contenido: 99,0 por ciento a 101,0 por ciento (sustancia anhidra).
PRODUCCIÓN
Dado que las N-nitrosaminas están clasificadas como probables carcinógenos humanos, se debe evitar o limitar en la medida de lo posible su presencia en candesartán cilexetilo. Por este motivo, se espera que los fabricantes de candesartán cilexetilo para uso humano realicen una evaluación del riesgo de formación de N-nitrosamina y contaminación durante su proceso de fabricación; Si esta evaluación identifica un riesgo potencial, se debe modificar el proceso de fabricación para minimizar la contaminación e implementar una estrategia de control para detectar y controlar las impurezas de N-nitrosamina en candesartán cilexetilo. El capítulo general 2.5.42. N-Nitrosaminas en sustancias activas está disponible para ayudar a los fabricantes.
PERSONAJES
Aspecto: polvo blanco o casi blanco.
Solubilidad: prácticamente insoluble en agua, fácilmente soluble en cloruro de metileno y ligeramente soluble en etanol anhidro.
Muestra polimorfismo (5.9).
IDENTIFICACIÓN
Espectrofotometría de absorción infrarroja (2.2.24).
Comparación: candesartán cilexetilo CRS.
Si los espectros obtenidos muestran diferencias, disolver la sustancia a examinar y la sustancia de referencia por separado en etanol anhidro R, evaporar hasta sequedad y registrar nuevos espectros utilizando los residuos.
PRUEBAS
Sustancias relacionadas. Cromatografía líquida (2.2.29). Prepare las soluciones inmediatamente antes de su uso.
Mezcla de disolventes: agua R, acetonitrilo R (40:60 V/V).
Solución de prueba. Disolver 20 mg de la sustancia a examinar en 50,0 ml de la mezcla de disolventes.
Solución de referencia (a). Diluir 1,0 ml de la solución de prueba a 100,0 ml con la mezcla de disolventes. Diluya 1,0 ml de esta solución a 10,0 ml con la mezcla de disolventes.
Solución de referencia (b). Disuelva 5 mg de candesartán cilexetilo para la idoneidad del sistema CRS (que contiene impurezas A, B y F) en la mezcla de disolventes y diluya hasta 10 ml con la mezcla de disolventes.
Solución de referencia (c). Disolver 2,5 mg de candesartán cilexetilo para la identificación del pico CRS (que contiene impurezas G y H) en la mezcla de disolventes y diluir a 5 ml con la mezcla de disolventes.
Columna:
- tamaño: l = 0,15 m, Ø = 3,9 mm;
- Fase estacionaria: gel de sílice octadecilsililo finalizado para
cromatografía R (4 μm).
Fase móvil:
- fase móvil A: ácido acético glacial R, agua para
cromatografía R, acetonitrilo R (1:43:57 V/V/V);
- fase móvil B: ácido acético glacial R, agua para
cromatografía R, acetonitrilo R (1:10:90 V/V/V);
Tiempo (min) Fase móvil A (porcentaje V/V) Fase móvil B (porcentaje V/V)
0 - 3 100 0
3 - 33 100 → 0 0 → 100
33 - 40 0 100
Caudal: 0,8 ml/min.
Detección: espectrofotómetro a 254 nm.
Inyección: 10 μL.
Identificación de impurezas: utilice el cromatograma suministrado con candesartán cilexetilo para la idoneidad del sistema CRS y el cromatograma obtenido con la solución de referencia (b) para identificar los picos debidos a las impurezas A, B y F; utilice el cromatograma suministrado con candesartán cilexetilo para la identificación de picos CRS y el cromatograma obtenido con la solución de referencia (c) para identificar los picos debidos a las impurezas G y H.
Retención relativa con referencia a candesartán cilexetilo
(tiempo de retención = aproximadamente 11 min): impureza G = aproximadamente 0,2;
impureza A = aproximadamente 0,4; impureza B = aproximadamente 0,5;
impureza F = aproximadamente 2,0; impureza H = alrededor de 3,5.
Idoneidad del sistema: solución de referencia (b):
- resolución: mínimo 4,0 entre los picos debido a las impurezas A y B.
Límites:
- factores de corrección: para el cálculo del contenido, multiplicar las áreas de los picos de las siguientes impurezas por el factor de corrección correspondiente: impurezas A y G = 0,7;
impureza H = 1,6;
- impureza B: no más de 3 veces el área del pico principal en el cromatograma obtenido con la solución de referencia (a) (0,3 %);
- impurezas F, G: para cada impureza, no más del doble del área del pico principal en el cromatograma obtenido con la solución de referencia (a) (0,2 %).
- impurezas A, H: para cada impureza, no más de 1,5 veces el área del pico principal en el cromatograma obtenido con la solución de referencia (a) (0,15 %);
- impurezas no especificadas: para cada impureza, no más que el área del pico principal en el cromatograma obtenido con la solución de referencia (a) (0,10 %);
- total: no más de 6 veces el área del pico principal en el cromatograma obtenido con la solución de referencia (a) (0,6 %);
- límite de desprecio: 0,5 veces el área del pico principal en el cromatograma obtenido con la solución de referencia (a) (0,05 %).
Agua (2.5.32): máximo 0,3 por ciento, determinado sobre 60,0 mg.
Cenizas sulfatadas (2.4.14): máximo 0,1 por ciento, determinado sobre 1,0 g.
ENSAYO
Disolver 0,500 g en 60 mL de ácido acético glacial R. Titular inmediatamente con ácido perclórico 0,1 M, determinando el punto final potenciométricamente (2.2.20) en el 1er punto de inflexión.
1 mL de ácido perclórico 0,1 M equivale a 61,1 mg de C33H34N6O6.
IMPUREZAS
Impurezas especificadas: A, B, F, G, H.
Otras impurezas detectables (las siguientes sustancias, si estuvieran presentes en un nivel suficiente, se detectarían mediante una u otra de las pruebas de la monografía. Están limitadas por el criterio de aceptación general para otras impurezas/no especificadas y/o por la monografía general Sustancias para uso farmacéutico (2034). Por lo tanto, no es necesario identificar estas impurezas para demostrar el cumplimiento. Véase también 5.10. Control de impurezas en sustancias para uso farmacéutico): C, D, E, I.
A. 2-etoxi-1-[[2′-(1H-tetrazol-5-il)bifenil-4-il]metil]-1H-bencimidazol-7-carboxilato,
B. (1RS)-1-[[(ciclohexiloxi)carbonil]oxi]etilo 2-oxo-3-[[2′-(1H-tetrazol-5-il)bifenil-4-il]metil]-2,3-dihidro-1H-bencimidazol-4-carboxilato,
C. (1RS)-1-[[(ciclohexiloxi)carbonil]oxi]etilo 3-[[2′-(1-etil-1H-tetrazol-5-il)bifenil-4-il]metil]-2-oxo-2,3-dihidro-1H-bencimidazol-4-carboxilato,
D. (1RS)-1-[[(ciclohexiloxi)carbonil]oxi]etilo 3-[[2′-(2-etil-2H-tetrazol-5-il)bifenil-4-il]metil]-2-oxo-2,3-dihidro-1H-bencimidazol-4-carboxilato,
E. (1RS)-1-[[(ciclohexiloxi)carbonil]oxi]etilo 2-etoxi-1-[[2′-(1-etil-1H-tetrazol-5-il)bifenil-4-il]metil]-1H-bencimidazol-7-carboxilato,
F. (1RS)-1-[[(ciclohexiloxi)carbonil]oxi]etilo 2-etoxi-1-[[2′-(2-etil-2H-tetrazol-5-il)bifenil-4-il]metil]-1H-bencimidazol-7-carboxilato,
G. 2-etoxi-1-[[2′-(1H-tetrazol-5-il)bifenil-4-il]metil]-1H-bencimidazol-7-ácido carboxílico (candesartán),
H. (1RS)-1-[[(ciclohexiloxi)carbonil]oxi]etilo 2-etoxi-1-[[2′-[1-(trifenilmetil)-1H-tetrazol-5-il]bifenil-4-il]metilo]-1H-bencimidazol-7-carboxilato
(N-tritilcandesartán),
I. 2-etoxi-1-[[2′-(1H-tetrazol-5-il)bifenil-4-il]metil]-1H-bencimidazol-7-carboxilato.